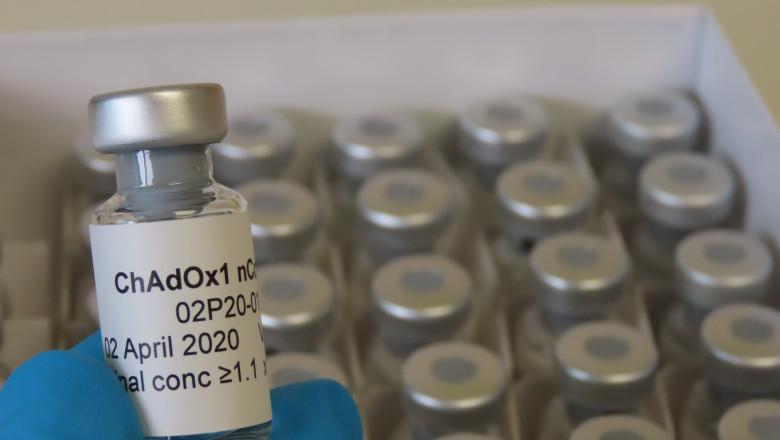
Agenţia Europeană pentru Medicamente (EMA) a anunţat marţi că a primit din partea companiei AstraZeneca o cerere de autorizare condiţionată pe piaţa europeană a vaccinului său, dezvoltat împotriva maladiei COVID-19 în colaborare cu Universitatea Oxford.
Reprezentanţii EMA au precizat că vor analiza solicitarea companiei britanice prin intermediul unei proceduri accelerate. O opinie despre o eventuală autorizare condiţionată ar putea fi enunţată pe 29 ianuarie, în timpul unei reuniuni a Comitetului pentru Medicamente de Uz Uman (CHMP) din cadrul Agenţiei. EMA a transmis, de asemenea, că în timpul procedurii sale de analizare continuă a vaccinului britanic a evaluat datele furnizate de studii aflate în desfăşurare în Marea Britanie, Brazilia şi Africa de Sud.
Dacă va primi recomandarea pentru utilizare din partea EMA şi va fi aprobat apoi în mod oficial de Comisia Europeană, vaccinul AstraZeneca-Oxford va deveni cel de-al treilea ser anti-COVID-19 care va fi disponibil în Europa, după cele produse de Pfizer-BioNTech şi Moderna.